Chapitre
Le corps humain : une usine chimique
Savoirs
Le nom et la formule des ions responsables de l'acidité et de la basicité
Plus il y a d'ions hydrogène plus une solution est acide
Plus il y a d'ions hydroxyde, plus une solution est basique
Savoir que les acides et les bases réagissent entre eux et que cela modifie le pH
Savoir qu'une transformation chimique peut libérer de l'énergie
Savoirs-faire
Mesurer un pH
Etablir un bilan réactionnel
Ecrire une formule à partir de sa composition atomique
Ecrire une équation de réaction
Déterminer si une équation de réaction est équilibrée
Equilibrer une équation de réaction
Compétences travaillées
1 Des langages pour penser et communiquer
2 Les méthodes et les outils pour apprendre
3 La formation de la personne et du citoyen
4 Les systèmes naturels et les systèmes techniques
Introduction

Le corps humain transforme les aliments selon des transformations chimiques,
quel type de transformation chimique met-il en jeu ?
I Rappels

Transformations....
II Des ions responsables
1 Activité
 Acidité, basicité ?
Acidité, basicité ?
 Acidité, basicité ?
Acidité, basicité ?
 Acidité, basicité ? - correction
Acidité, basicité ? - correction
2 A retenir
Les solutions acides (pH<7)et basiques (pH>7 ) contiennent des ions.
Les ions hydrogènes H+ sont responsables de l’acidité des solutions, pour un même volume de solution, plus il y a d’ions H+, plus la solution est acide.
Les ions hydroxydes HO- sont responsables de la basicité des solutions, pour un même volume de solution, plus il y a d’ions HO-, plus la solution est basique.
Lorsque l’on dilue une solution acide son pH augmente jusqu’à 7 sans dépasser cette valeur, pour les solutions basiques, le pH diminue jusqu’ à 7 sans aller au-dessous.
III Des transformations chimiques dans le corps
1 Activité
 Réactions acide-base.
Réactions acide-base.
 Réactions acide-base.
Réactions acide-base.
 Réactions acide-base.- correction
Réactions acide-base.- correction
3 A retenir
Les acides et les bases réagissent l'un avec l'autre.
Au cours de cette transformation chimique les réactifs, l'acide et la base sont transformés en de nouveaux produits dont de l'eau.
Base + acide - > eau + produits
Comme pour toute transformation chimique, la masse est conservée, donc il y a le même nombre d'atomes de chaque sorte dans les réactifs et les produits, mais les charges électriques également.
Exemple : réaction entre l'acide chlorhydrique et le bicarbonate de sodium
H+ + Cl-+ HCO3- + Na+ > NaCl + CO2 + H2O
IV Phénomène de corrosion
1 Activité
 corrosion
corrosion
 corrosion
corrosion
 corrosion.- correction
corrosion.- correction
3 A retenir
Les acides et les bases réagissent l'un avec l'autre.
Au cours de cette transformation chimique les réactifs, l'acide et la base sont transformés en de nouveaux produits dont de l'eau.
Base + acide - > eau + produits
Comme pour toute transformation chimique, la masse est conservée, donc il y a le même nombre d'atomes de chaque sorte dans les réactifs et les produits, mais les charges électriques également.
Exemple : réaction entre l'acide chlorhydrique et le bicarbonate de sodium
H+ + Cl-+ HCO3- + Na+ > NaCl + CO2 + H2O
IV Quelle énergie!!
1 Activité 'rappels sur les combustions
 Combustion du glucose.
Combustion du glucose.
 combustion du glucose.
combustion du glucose.
 Combustion du glucose. - correction
Combustion du glucose. - correction
3 A retenir
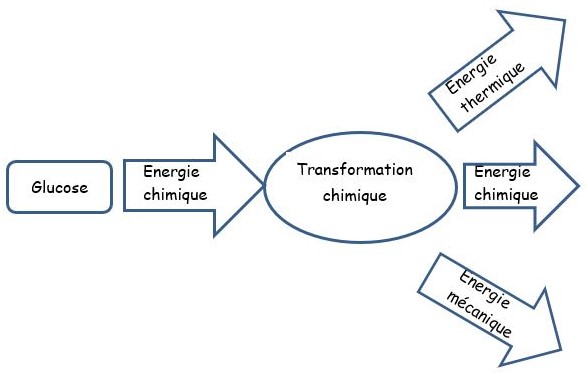
L’énergie nécessaire lors d’une activité physique ou tout simplement pour maintenir la température
de 37°C provient d’une transformation chimique qui s’apparente à la combustion du glucose.
C6H12O6 + 6 O2 > 6CO2 + 6 H2O
L'énergie chimique du glucose est transformée en énergie mécanique, chimique ou thermique.
Chaîne énergétique


 Transformations....
Transformations....
 Acidité, basicité ?
Acidité, basicité ?
 Acidité, basicité ?
Acidité, basicité ?
 Acidité, basicité ? - correction
Acidité, basicité ? - correction
 Réactions acide-base.
Réactions acide-base.
 Réactions acide-base.
Réactions acide-base.
 Réactions acide-base.- correction
Réactions acide-base.- correction
 corrosion
corrosion
 corrosion
corrosion
 corrosion.- correction
corrosion.- correction
 Combustion du glucose.
Combustion du glucose.
 combustion du glucose.
combustion du glucose.
 Combustion du glucose. - correction
Combustion du glucose. - correction
